Quarto studio congiunto inter-agenzia sull’analisi integrata dei dati sul consumo di antimicrobici e sullo sviluppo di resistenza agli antimicrobici nei batteri presenti in esseri umani e in animali da reddito nell’Unione europea (JIACRA IV, 2019-2021)
Clausola di esclusione della responsabilità
- La presente pubblicazione è una sintesi semplificata del quarto studio congiunto inter-agenzia condotto da ECDC, EFSA ed EMA sull’analisi integrata dei dati sul consumo di antimicrobici e sullo sviluppo di resistenza agli antimicrobici nei batteri presenti in esseri umani e in animali da reddito nell’UE e nel SEE. La versione integrale dello studio è disponibile qui.
- La presente sintesi semplificata è intesa a migliorare la trasparenza e a informare le parti interessate in merito al lavoro svolto dall’ECDC, dall’EFSA e dall’EMA sull’argomento presentando una sintesi dei principali risultati in un linguaggio più semplice.
Contesto
- La resistenza agli antimicrobici (antimicrobial resistance, AMR) è un grave problema di portata mondiale per la salute umana e animale.
- L’uso, proprio e improprio, di antimicrobici negli esseri umani e negli animali da reddito sono i fattori principali all’origine dell’AMR, un fenomeno che va affrontato mediante il coordinamento di misure nei settori della salute umana e di quella animale in tutto il mondo.
- Le infezioni batteriche resistenti agli antimicrobici sono un grave problema sanitario in Europa in quanto causano oltre 35 000 decessi l’anno, una cifra paragonabile alle conseguenze di influenza, tubercolosi e HIV/AIDS messi insieme. In base a dati recenti, i batteri resistenti agli antimicrobici stanno causando un numero crescente di infezioni e decessi negli esseri umani, in particolare nelle strutture sanitarie.
- In conformità del piano d’azione europeo «One Health» contro la resistenza agli antimicrobici, la Commissione europea (CE) ha incaricato il Centro europeo per la prevenzione e il controllo delle malattie (ECDC), l’Autorità europea per la sicurezza alimentare (EFSA) e l’Agenzia europea per i medicinali (EMA) di acquisire dati sul collegamento tra il consumo di antimicrobici (antimicrobial consumption, AMC) e l’AMR in esseri umani e animali da reddito.
- Il presente documento è il quarto studio congiunto inter-agenzia sull’analisi integrata dei dati sul consumo di antimicrobici e sullo sviluppo di AMR (Joint Interagency Antimicrobial Consumption and Resistance Analysis, JIACRA), che ha per oggetto principalmente il periodo 2019-2021. Le tre precedenti edizioni dello studio JIACRA hanno preso in esame i dati relativi ad AMC e AMR per una serie di periodi consecutivi a partire dal 2011.
Che cosa è stato chiesto di fare all’ECDC, all’EFSA e all’EMA?
- La Commissione europea ha incaricato l’ECDC, l’EFSA e l’EMA di condurre il quarto studio JIACRA, che presenta i risultati delle analisi dei dati derivanti da ricerche sulle possibili correlazioni tra AMC in esseri umani e animali da reddito e la presenza di AMR nei batteri in entrambi i settori. Le analisi erano inoltre mirate a individuare eventuali tendenze significative nelle manifestazioni di AMR e AMC nonché a valutare se tali tendenze fossero concomitanti.
In che modo l’ECDC, l’EFSA e l’EMA hanno svolto il lavoro?
- Il quarto studio JIACRA è stato condotto prendendo in considerazione diverse serie di dati provenienti dai programmi di sorveglianza e monitoraggio a livello dell’UE aventi per oggetto l’AMR e l’AMC in esseri umani e animali da reddito nell’Unione europea (UE) e nello Spazio economico europeo (SEE), programmi coordinati rispettivamente dall’ECDC, dall’EFSA e dall’EMA. I dati acquisiti dal 2019 al 2021 hanno costituito la base principale per l’analisi (figura I).
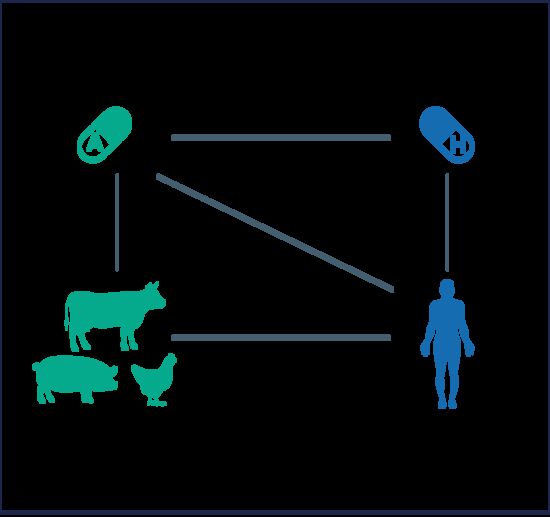
Figura I. Potenziali collegamenti studiati tra il consumo di antimicrobici negli esseri umani e negli animali da reddito e resistenza agli antimicrobici nei batteri presenti nell’uomo e negli animali da reddito
- Per analizzare e confrontare i dati relativi all’AMC sono stati aggregati dati sul consumo totale di antimicrobici nei paesi UE/SEE al fine di calcolare un consumo medio in milligrammi di antimicrobici per chilogrammo di biomassa stimata in esseri umani e animali da reddito. È possibile che alcuni aspetti tecnici minori nelle diverse metriche utilizzate nell’ambito dei programmi specifici di sorveglianza dell’AMC negli esseri umani e negli animali da reddito abbiano inciso in termini di perfetta comparabilità tra i settori.
- Per esaminare le possibili associazioni tra AMC e AMR è stata condotta una serie di analisi su specifiche combinazioni di batteri e classi di antimicrobici basata sui dati di sorveglianza disponibili con riferimento al settore sia umano sia animale. Le combinazioni selezionate, classificate in ordine di priorità in base alla loro rilevanza per la salute pubblica, hanno interessato quattro batteri e sette classi di antimicrobici (figura II). Gli isolati batterici umani provenivano da soggetti clinicamente malati sottoposti a campionamento in strutture sanitarie, mentre quelli di animali da reddito erano stati prelevati al momento della macellazione da animali sani allevati in ambito nazionale.
- Sono state utilizzate le stesse fonti di dati e le stesse metriche dei precedenti studi JIACRA, cosa che ha facilitato l’analisi relativa al periodo 2014-2021 intesa a individuare eventuali tendenze significative e a confrontare quelle dell’AMC e dell’AMR nei vari paesi valutando se tali tendenze fossero concomitanti.
Quali sono stati i risultati e le relative implicazioni?
- Nel 2021 l’AMC complessiva in 29 paesi UE/SEE è stata valutata a 125,0 mg per kg di biomassa (28 paesi, intervallo 44,3-160,1) per gli esseri umani e a 92,6 mg per kg di biomassa per gli animali da reddito (29 paesi, intervallo 2,5-296,5).
- Tra il 2014 e il 2021 la media dell’AMC complessiva in mg/kg negli animali da reddito è diminuita del 44 %, mentre negli esseri umani è rimasta relativamente stabile. L’AMC è risultata variare notevolmente tra i paesi dell’UE/SEE nei quali per la maggior parte (se non in tutti) si evidenziava una tendenza al ribasso. Tale dato dimostra che le misure attuate per ridurre l’AMC negli animali da reddito e negli esseri umani sono risultate efficaci in molti paesi. Tuttavia, tali misure devono essere rafforzate per poter continuare a osservare nonché ad accentuare ulteriormente tali riduzioni, ove necessario. Sarebbero necessari ulteriori interventi per ridurre l’uso non necessario di antimicrobici negli esseri umani. Una maggiore completezza nella comunicazione dei dati relativi all’AMC negli esseri umani nel corso del periodo oggetto di studio potrebbe, tuttavia, aver celato eventuali ulteriori riduzioni.
- Tra il 2014 e il 2021, in 10 dei 20 paesi nei quali è stata ridotta in modo significativo l’incidenza complessiva di AMC negli animali da reddito, il batterio intestinale indicatore E. coli isolato da animali da reddito è risultato sempre più sensibile agli antimicrobici (nel senso che ha evidenziato «sensibilità completa» o «resistenza zero» a una serie armonizzata di antimicrobici molto diffusi). Analogamente, in nove dei 19 paesi nei quali è stata ridotta in modo significativo l’incidenza complessiva di AMC negli esseri umani, l’ E. coli isolato da infezioni invasive umane è risultato sempre più sensibile (nel senso che ha evidenziato «sensibilità completa» o «resistenza zero» a una serie armonizzata di antimicrobici molto diffusi). Questi risultati dimostrano che una riduzione generale dell’AMC può contribuire a ridurre l’AMR, oltre a evidenziare l’importanza dell’adozione di misure che promuovano la salute umana e animale, come la vaccinazione e una migliore igiene, riducendo così la necessità di somministrare antimicrobici.
- I dati dal 2019 al 2021 hanno confermato un collegamento tra i livelli di consumo di determinate classi di antimicrobici e la comparsa di AMR alle suddette classi di antimicrobici in batteri presenti sia nell’essere umano sia in animali da reddito (figura II):
- nell’uomo sono state riscontrate associazioni positive tra il livello di AMC in carbapenemi, cefalosporine di terza e quarta generazione e (fluoro)chinoloni e la resistenza a ognuna di queste classi in E. coli isolato da infezioni invasive umane.
- Negli animali da reddito sono state evidenziate associazioni positive tra il livello di AMC in (fluoro)chinoloni, polimixine, aminopenicilline e tetracicline e la resistenza a ognuna di queste classi dell’indicatore E. coli isolato da animali da reddito.
- Nel pollame i livelli di consumo di (fluoro)chinoloni sono stati positivamente associati a quelli di resistenza a questa classe di antimicrobici in Campylobacter jejuni.
- Nei suini i livelli di consumo di (fluoro)chinoloni e macrolidi sono stati positivamente associati a quelli di resistenza alle rispettive classi in Campylobacter coli.
- In alcuni casi l’AMR nei batteri isolati dall’uomo è stata collegata anche ad AMR in batteri isolati da animali da reddito, a loro volta associati alla corrispondente AMR negli stessi animali da reddito, in particolare per le combinazioni di batteri zoonotici di origine alimentare come Campylobacter jejuni e (fluoro)chinoloni o di Campylobacter coli e macrolidi.
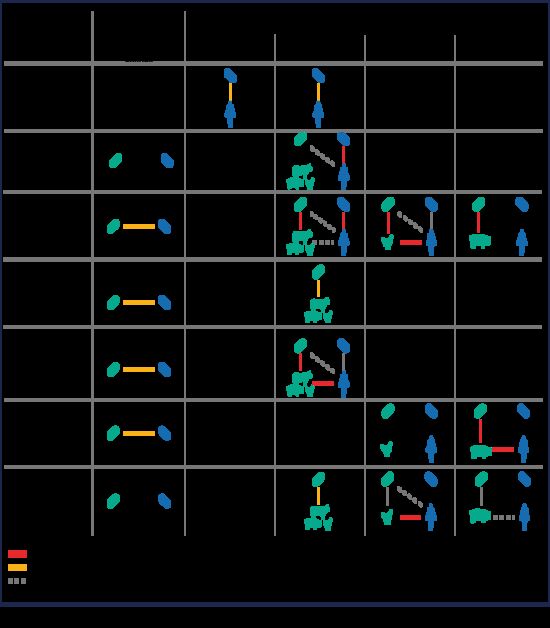
Figura II. Collegamenti individuati in sede di analisi tra il consumo di antimicrobici (AMC) in esseri umani e animali da reddito e resistenza agli antimicrobici (AMR) in batteri isolati da esseri umani e animali da reddito
- Per quanto riguarda gli animali da reddito, nel periodo 2014-2021 si sono registrate riduzioni statisticamente significative del consumo di cefalosporine di terza e quarta generazione, di chinoloni, di polimixine, di aminopenicilline e di tetracicline in almeno un quarto dei Paesi presi in esame. Per la maggior parte di questi Paesi tale riduzione è risultata accompagnarsi a una tendenza al ribasso, in misura spesso statisticamente significativa, della resistenza alla classe correlata di antimicrobici in batteri di E. coli prelevati da campioni di intestino di animali.
- Nello stesso periodo si sono registrate tendenze statisticamente significative relative a una riduzione del consumo umano di chinoloni e aminopenicilline per almeno due terzi dei Paesi presi in esame. Per almeno un quarto di essi tale tendenza al ribasso si è accompagnata a una tendenza statisticamente significativa alla riduzione della resistenza a queste classi di antimicrobici in batteri di E. coli prelevati in un contesto di infezioni invasive in esseri umani.
- In 11 Paesi è stato evidenziato un aumento statisticamente significativo del consumo di carbapenemi nell’uomo (nella maggior parte dei casi a partire da livelli molto bassi). Non sono state rilevate tendenze statisticamente significative relativamente al consumo di cefalosporine di terza e quarta generazione negli esseri umani.
- Tali dati sottolineano ulteriormente la necessità di un monitoraggio integrato continuo dell’AMC e dell’AMR associato a interventi volti a promuovere un uso più oculato di tutti gli antimicrobici, in particolare di quelli che rivestono un’importanza primaria in medicina umana.
Quali sono le raccomandazioni principali?
- Sono necessari interventi continui e coordinati per giungere, entro il 2030, a una riduzione del 20 % dell’AMC negli esseri umani (rispetto ai livelli del 2019) e del 50 % negli animali da reddito (rispetto ai livelli del 2018), come raccomandato nel primo caso dal Consiglio dell’Unione europea e come previsto, nel secondo, dalla strategia «Dal produttore al consumatore», anche mediante una formazione specifica di operatori sanitari e veterinari.
- È opportuno attuare iniziative specifiche per ridurre e limitare l’AMR nel suo complesso nei settori sia umano sia animale, dal momento che le riduzioni dell’AMC complessiva sono state associate a riduzioni dell’AMR, anch’essa nel suo complesso. Particolare attenzione dovrebbe essere prestata anche alla limitazione dell’uso degli antimicrobici di importanza primaria (in base alla definizione del gruppo di esperti ad hoc dell’EMA sulla consulenza per gli antimicrobici) in medicina umana.
- È fondamentale concentrarsi maggiormente sulle misure preventive e sul controllo delle infezioni per ridurre la necessità di somministrare trattamenti antimicrobici e per prevenire la diffusione dell’AMR.
- Dovrebbe essere garantito un uso responsabile e oculato degli antimicrobici accompagnato da misure atte a migliorare la disponibilità e l’accessibilità di test diagnostici e di orientamenti in materia di trattamento nonché a migliorare il livello di conformità agli stessi.
- Dovrebbero essere acquisiti dati complementari atti a permettere una migliore analisi delle relazioni tra l’AMC e l’AMR attraverso una sorveglianza integrata e armonizzata dei due fenomeni in entrambi i settori, umano e animale. In base a un approccio «One Health», in tale analisi potrebbero essere integrati anche i dati relativi al settore ambientale, non appena disponibili.
- Sono necessari ulteriori studi mirati per esaminare e comprendere meglio la trasmissione di batteri antimicrobico-resistenti e di geni dell’AMR tra animali ed esseri umani, oltre che nell’ambiente.

Figura III. Panoramica delle principali raccomandazioni
Glossario
Resistenza agli antimicrobici: la capacità dei microrganismi di sopravvivere o crescere in presenza di una concentrazione di un agente antimicrobico che è generalmente sufficiente a inibire o uccidere microrganismi della stessa specie [articolo 4, punto 11, del regolamento (UE) 2019/6].
«Sensibilità completa» o «resistenza zero»: tecnicamente, la sensibilità a tutte le classi di antimicrobici inclusi nei pannelli armonizzati di antimicrobici trattati nell’ambito di un monitoraggio (i pannelli sono presentati nello studio).
Risorse sul tema
Raccolta degli studi JIACRA nell’EFSA Journal
Piano d’azione europeo «One Health» contro la resistenza agli antimicrobici
Risorse web dell’EFSA sull’AMR
Risorse web dell’EMA
Sorveglianza europea sull'impiego di antimicrobici in campo veterinario (ESVAC): 2009-2023
Pagina sull’analisi dell'impiego di antimicrobici e della resistenza agli antimicrobici
Risorse web dell’ECDC
Dashboard sul consumo di antimicrobici
Relazioni sul consumo di antimicrobici
Dati sulla resistenza agli antimicrobici
Relazioni sulla resistenza agli antimicrobici
https://www.ecdc.europa.eu/en/antimicrobial-resistance/surveillance-and-disease-data
https://www.ecdc.europa.eu/en/campylobacteriosis/antimicrobial-resistance
Riferimento bibliografico
Centro europeo per la prevenzione e il controllo delle malattie (ECDC), Autorità europea per la sicurezza alimentare (EFSA) e Agenzia europea per i medicinali (EMA) Quarto studio congiunto inter-agenzia sull’analisi integrata dei dati sul consumo di antimicrobici e sullo sviluppo di resistenza agli antimicrobici nei batteri presenti negli esseri umani e in animali da reddito nell’UE/SEE Stoccolma, Parma, Amsterdam: ECDC/EFSA/EMA, 2024. DOI: https://doi.org/10.2903/j.efsa.2024.8589
ISSN: 1831-4732
© Autorità europea per la sicurezza alimentare, 2022
Riproduzione autorizzata con citazione della fonte.